Из курса физики в 7 классе мы знаем, что вода – вещество, чрезвычайно важное для Земли. Внешний вид нашей планеты и сама жизнь на ней определяется наличием воды во всех трех агрегатных состояниях. Давайте поговорим об удивительных свойствах воды, которые сделали ее столь важной для нашего существования.
Молекула воды
Молекула воды представляет собой соединение двух атомов водорода с одним атомом кислорода. Электронная оболочка атома водорода имеет один электрон, а внешняя оболочка атома кислорода — шесть электронов. Двум атомам водорода «энергетически выгодно» объединить свою оболочку с атомом кислорода, в результате чего образуется общая восьмиэлектронная оболочка.
Из-за большой разницы зарядов ядер электроны в этой оболочке распределены неравномерно. Большая часть электронов расположена вблизи атома кислорода, что создает асимметрию молекулы. Молекула имеет форму равнобедренного треугольника с острым углом примерно 105 ⁰.
Асимметрия распределения заряда (говорят «полярность» молекулы) определяет способность воды образовывать межмолекулярные связи (называемые водородными связями). В результате вода приобретает ряд интересных свойств.
Свойства воды
Важнейшим свойством воды является ее способность растворять многие вещества. Молекулы веществ, попадающих в раствор, окружаются полярными молекулами воды, которые не позволяют молекулам вернуться в исходное тело, и вещество начинает растворяться. В растворе молекулы веществ становятся более «свободными», в результате становятся возможными многие химические реакции, не протекающие между твердыми веществами.
Лимонная кислота и пищевая сода не вступают в реакцию друг с другом в виде порошка. Но если залить смесь порошка водой, начнется бурная реакция.
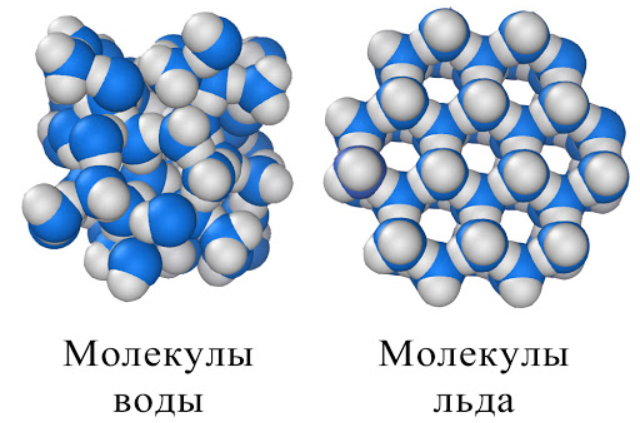
Вода проявляет более любопытное свойство, когда затвердевает. Всем известно по опыту, что лед плавает на поверхности воды, хотя большинство веществ в твердом состоянии увеличивают свою плотность. Поэтому плотность льда меньше. Почему?
Все дело опять же в образовании водородных связей. При образовании льда молекулы воды образуют водородные связи и располагаются в «ажурной» структуре. Плотность льда оказывается меньше плотности воды.
Рис. 2. Молекулы льда и воды.
Термальные свойства воды не менее удивительны. Они также определяются водородными связями. Их строительство и разрушение требуют дополнительной энергии, поэтому вода имеет аномально высокую теплоемкость и теплоту парообразования.
Значение воды для жизни
Сложные свойства воды делают ее незаменимой для существования жизни на Земле. По сути, живые существа представляют собой «растворы» в клетках «пробирки», состоящих из белковых оболочек. В каждой «пробирке» происходит множество биохимических реакций при непосредственном участии воды.
Во время фотосинтеза растения синтезируют глюкозу из углекислого газа и воды и выделяют кислород. Однако атомы кислорода, выделяемые растениями, изначально входят в состав молекул воды. Атомы кислорода, входящие в состав поглощаемой молекулы углекислого газа, превращаются в молекулы глюкозы и усваиваются растениями.
Что мы узнали
Молекула воды состоит из одного атома кислорода и двух атомов водорода и способна образовывать связи, называемые водородными связями. Это, в свою очередь, определяет способность воды растворять другие вещества, иметь высокую теплоемкость и низкую плотность в твердом состоянии. Кроме того, жизнь невозможна без воды.