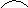- Сопряжение работы дыхательной цепи с процессом синтеза атф
- Разобщение дыхания и фосфорилирования
- Механизм сопряжения окисления и фосфорилирования
- Для чего образуются восстановленные НАД и ФАД?
- Окислительное фосфорилирование
- Принцип работы дыхательной цепи
- Цепь переноса электронов (цпэ), сопряжение дыхания и синтеза атф в митохондриях, коэффициент окислительного фосфорилирования. Ингибиторы и разобщители цпэ.
- Окислительное декарбоксилирование пировиноградной кислоты: схема процесса, связь с синтезом атф. Строение пируватдегидрогеназного комплекса: ферменты, коферменты, регуляция процесса.
- Цикл трикарбоновых кислот (цтк). Биологическая роль.
- Регуляция и анаболическая функция цтк.
- 1.3. Обмен углеводов
- Пищевые углеводы. Схема переваривания углеводов в жкт. Причины непереносимости молока.
Сопряжение работы дыхательной цепи с процессом синтеза атф
Существует несколько гипотез, объясняющих механизм сопряжения. Одной из них является хемоосмотическая теория. Цепь транспорта электронов функционирует как протонная (Н+)помпа, осуществляя перенос протонов из матрикса через внутреннюю мембрану в межмембранное пространство. Эндоэргический процесс выброса протонов из матрикса возможен за счет экзоэргических окислительно-восстановительных реакций дыхательной цепи. Перенос протонов приводит к возникновению разности концентрации Н+ с двух сторон митохондриальной мембраны: более высокая концентрация будет снаружи и более низкая — внутри. Митохондрия в результате переходит в «энергизованное» состояние, так как возникает градиент концентрации Н+ и одновременно разность электрических потенциалов со знаком плюс на наружной поверхности.
Электрохимический потенциал способен совершать «полезную» работу, он заставляет протоны двигаться в обратном направлении, но мембрана непроницаема для них кроме отдельных участков, называемых протонными каналами. Обратный перенос протонов в матрикс является экзоэргическим процессом, высвобождающаяся при этом энергия используется на фосфорилирование ADP. Эту реакцию катализирует фермент Н+-АТР-синтетаза, располагающаяся в области протонных каналов на внутренней поверхности внутренней мембраны. [2]
Разобщение дыхания и фосфорилирования
Сопряжение между дыханием и синтезом АТФ может быть нарушено разобщителями. Разобщители нарушают дыхательный контроль (т.е. стимулируют дыхание в отсутствие синтеза АТФ) и стимулируют гидролиз АТФ в митохондриях.Некоторые химические вещества (протонофоры) могут переносить протоны или другие ионы (ионофоры) из межмембранного пространства через мембрану в матрикс, минуя протонные каналы АТФ-синтазы. В результате этого исчезает электрохимический потенциал и прекращается синтез АТФ. Это явление называют разобщением дыхания и фосфорилирования. В результате разобщения количество АТФ снижается, а АДФ увеличивается. В этом случае скорость окисления NADH и FADH2 возрастает, возрастает и количество поглощённого кислорода, но энергия выделяется в виде теплоты, и коэффициент Р/О резко снижается. [3]
Разобщающее действие вызывает специфический фермент — аденозинтрифосфатаза, а также другие фосфатазы. Существуют и специфические ингибиторы (яды) окислительного фосфорилирования — так называемые разобщающие агенты или факторы. Типичным представителем последних является динитрофенол, механизм действия которого заключается, в конечном итоге, в стимулировании фосфатазной активности клетки. Динитрофенол и аналогичные ему агенты (например, дикумарол, арсениты) не затрагивают природы самих компонентов, участвующих в процессе фосфорилирования. Их действие заключается только в гидролизе макроэргических связей в молекуле АТФ или не содержащих фосфора предшественников последней. Наряду с этим имеется группа ингибиторов фосфорилирования, действие которых основано на связывании компонентов, участвующих в транспорте электронов по цепи. Таковы цианиды, амитал, антимицин и др. Известны, наконец, агенты, ингибирующее действие которых распространяется на соединения, участвующие в сопряжении окисления с фосфорилирование. Некоторые из ингибиторов оказывают комплексное воздействие. [4]
Примерами разобщителей могут быть также некоторые лекарства, например дикумарол — антикоагулянт или метаболиты, которые образуются в организме, билирубин — продукт катаболизма, тироксин — гормон щитовидной железы Все эти вещества проявляют разобщающее действие только при их высокой концентрации.
Тироксин, также обладающий разобщающим действием, вызывает набухание митохондрий, увеличивает проницаемость митохондриальной мембраны. Часть субстратов цикла Кребса выходит в гиалоплазму. Окисление их ферментами гиалоплазмы при участии экстрамитохондриального НАД приводит к увеличению образования тепла в результате свободного окисления. Выработка АТФ в клетке уменьшается.
При разобщении окисления и фосфорилирования наблюдается несоответствие между данными прямой и непрямой калориметрий. При отравлении 2,4-а-динитрофенолом теплопродукция по калориметру может на 50-80% превышать рассчитанную по газообмену. При тиреотоксикозе теплопродукция по калориметру может превышать рассчитанную по газообмену на 20-40%.
Источник
Механизм сопряжения окисления и фосфорилирования
Перепад потенциалов от Н2 до О2 составляет 1,24 В, что теоретически достаточно для синтеза 6 молекул АТФ, однако реально синтезируется не более трёх.


АТФ образуется путём присоединения к АДФ остатка фосфорной кислоты. Этот процесс называется фосфорилированием. Таким образом, два процесса: процесс биологического окисления (передача протонов и электронов по дыхательной цепи) и процесс фосфорилирования (образование АТФ) являются сопряжёнными, так как энергия, образующаяся при окислении, используется для фосфорилирования. Поэтому образование АТФ за счёт энергии, выделяющейся при прохождении электронов по дыхательной цепи, называется окислительным фосфорилированием.
Для количественной характеристики сопряжения окисления и фосфорилирования используется коэффициент фосфорилирования – отношение Р/О. Этот коэффициент показывает, какое количество атомов неорганического фосфора поглощается митохондрией при поглощении одного атома кислорода (или при переносе одной пары электронов на кислород).
Расчёты показывают, что для образования одной макроэргической связи АТФ, затраты на которую составляют не менее 40 кДж/моль, требуется перепад окислительно-восстановительных потенциалов между участниками дыхательной цепи примерно в 0,22 В на пару перенесённых электронов. В дыхательной цепи имеются только три участка с разницей о/в потенциалов, достаточной для синтеза АТФ (три участка сопряжения окисления и фосфорилирования):
II – между цитохромами b и c;
На данных этапах выделение энергии достаточно для синтеза АТФ. На остальных этапах перепад о/в потенциалов недостаточен для синтеза АТФ и выделяющаяся энергия (около 40-50%) рассеивается в виде тепла. Таким образом, при прохождении двух электронов по дыхательной цепи, которая начинается НАД-зависимыми дегидрогеназами образуется три молекулы АТФ. В этом случае коэффициент Р/О = 3.
Некоторые субстраты окисления (сукцинат, жирные кислоты) имеют более высокий окислительно-восстановительный потенциал, чем НАД. Поэтому они окисляются не НАД-, а ФАД-зависимыми дегидрогеназами. При окислении таких веществ образуется только две молекулы АТФ, так как пропускается один пункт сопряжения окисления и фосфорилирования. Поэтому коэффициент Р/О = 2.
Приведённые значения коэффициентов фосфорилирования являются расчетными, реальное значение этого коэффициента в физиологических условиях составляет Р/О ≈ 2,5.
Коэффициент Р/О может иметь ещё более низкие значения (Р/О 3 / 6 3456> Следующая >>>
Источник
Для чего образуются восстановленные НАД и ФАД?
Молекулы НАДН и ФАДН2, образуемые в реакциях окисления углеводов, жирных кислот, спиртов и аминокислот, далее поступают в митохондрии, где ферментами дыхательной цепи осуществляется процесс окислительного фосфорилирования.
Окислительное фосфорилирование
Окислительное фосфорилирование – это многоэтапный процесс, происходящий во внутренней мембране митохондрий и заключающийся в окислении восстановленных эквивалентов (НАДН и ФАДН2) ферментами дыхательной цепи и сопровождающийся синтезом АТФ.
Впервые механизм окислительного фосфорилирования был предложен Питером Митчеллом. Согласно этой гипотезе перенос электронов, происходящий во внутренней митохондриальной мембране, вызывает выкачивание ионов Н + из матрикса митохондрий в межмембранное пространство. Это создает градиент концентрации ионов Н + между цитозолем и замкнутым внутримитохондриальным пространством. Ионы водорода способны возвращаться в матрикс митохондрий через специальный фермент, образующий АТФ – АТФ-синтазу.
Принцип работы дыхательной цепи
В целом работа дыхательной цепи заключается в следующем:
- Образующиеся в реакциях катаболизма НАДН и ФАДН2 передают атомы водорода (т.е. протоны водорода и электроны) на ферменты дыхательной цепи.
- Электроны движутся по ферментам дыхательной цепи и теряют энергию.
- Эта энергия используется на выкачивание протонов Н + из матрикса в межмембранное пространство.
- В конце дыхательной цепи электроны попадают на кислород и восстанавливают его до воды.
- Протоны Н + стремятся обратно в матрикс и проходят через АТФ-синтазу.
- При этом они теряют энергию, которая используется для синтеза АТФ.
Источник
Цепь переноса электронов (цпэ), сопряжение дыхания и синтеза атф в митохондриях, коэффициент окислительного фосфорилирования. Ингибиторы и разобщители цпэ.
Перенос электронов на кислород происходит при участии системы переносчиков, локализованных во внутренней мембране митохондрий и образующих цепь переноса электронов (ЦПЭ)
Энергия, обращающаяся при прохождении потока электронов по дыхательной цепи, используется для сопряженного фосфорилирования АДФ, причём окисление не протекает в отсутствии АДФ. Соотношение окисления и фосфорилирования определяется коофициентом фосфорилирования.
Коэффициент окислительного фосфорилирования (К) – это отношение количества неорганического фосфата, потребляемого в процессе дыхания, к количеству кислорода
Ингибиторы, блокирующие дыхательную цепь: барбитураты, ротенон — ингибиторы NADH-дегидрогеназы
Разобщители окислительного фосфорилирования:
-большие дозы йодсодержащих гормонов щитовидной железы
Окислительное декарбоксилирование пировиноградной кислоты: схема процесса, связь с синтезом атф. Строение пируватдегидрогеназного комплекса: ферменты, коферменты, регуляция процесса.
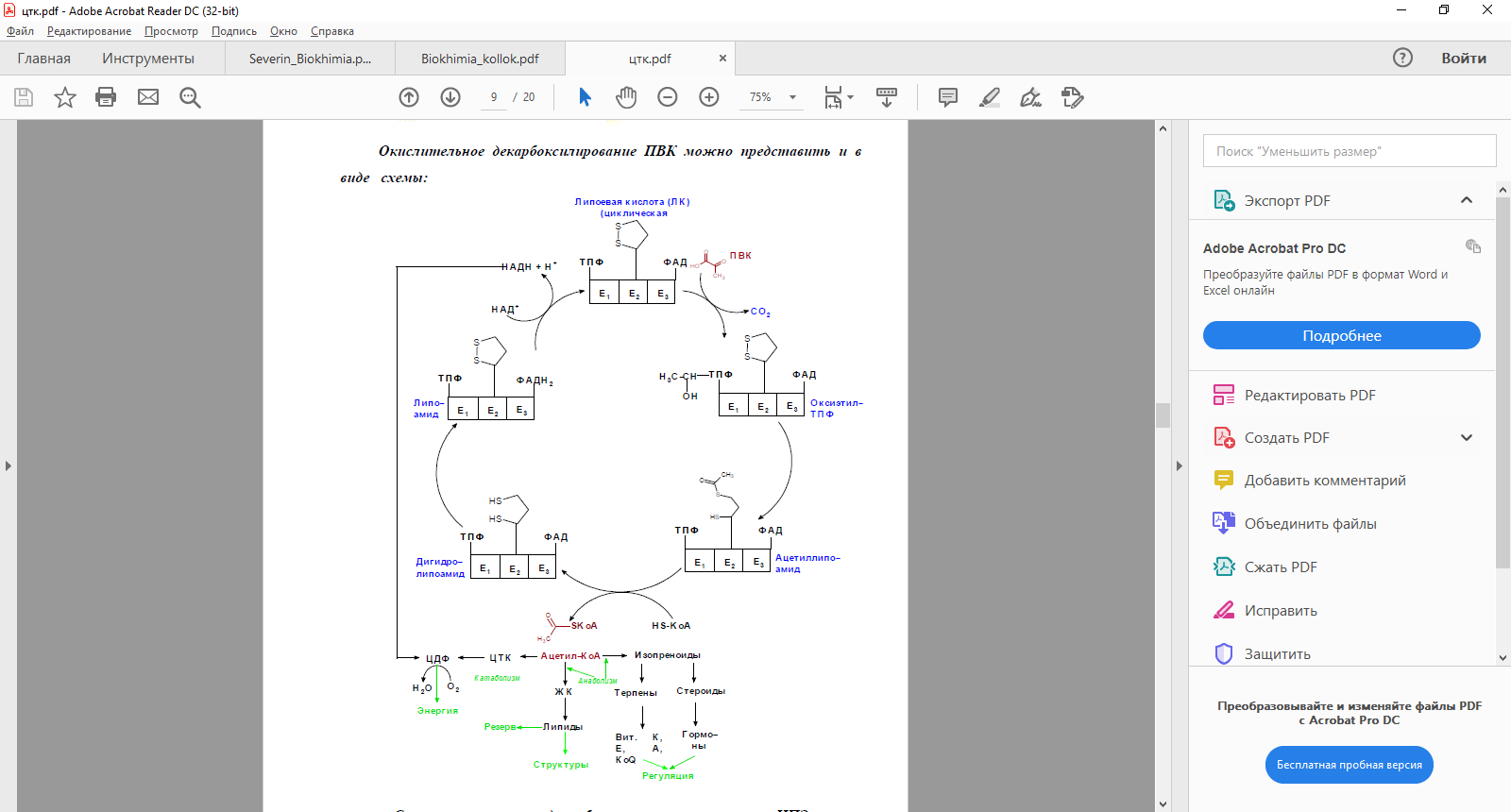
Связь окислительного декарбоксилирования пирувата с ЦПЭ
Окислительное декарбоксилирование пирувата сопровождается образованием NADH, поставляющим электроны в дыхательную цепь и обеспечивающим синтез 3 молей АТФ на 1 моль пирувата путём окислительного фосфорилирования .
Состав пируватдегидрогеназного комплекса входит 3 фермента и 5 коферментов
Е1- пируватдегидрогеназа. Кофермент- тиаминдифосфат
Е2- дигидролипоилтрансацетилаза. Кофермент – амид липоевой кислоты
Е3 – дигидролипоилдегидрогеназа. Кофермент- ФАД
HSKoА – кофермент ацилирования ( активная форма витамина В3)
НАД+- никотинамид аденин динуклеотид (активная форма витамина РР или В2)
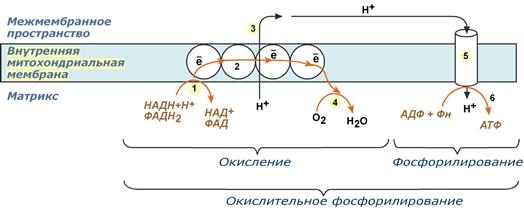
Цикл трикарбоновых кислот (цтк). Биологическая роль.
Цикл Кребса объединяет пути катаболизма углеводов, белков и жировобразующиеся при расщеплении этих веществ.
превращение различных веществ в субстраты цикла:
использование субстратов цикла на синтез органических веществ
цикл Кребса поставляет ЦПЭ протоны в виде трех НАДН+Н + и одного ФАДН2.
Регуляция и анаболическая функция цтк.
Лимитирующим ферментом ЦТК является изоцитратдегидрогеназа. Он активируется АДФ, НАД+, ингибируется АТФ, восстановленной формой НАДН•Н+.
Анаболические процессы приводят к снижению концентрации промежуточных продуктов цикла трикарбоновых кислот. Они быстро истощают пул промежуточных продуктов цикла. Поэтому их запас постоянно пополняется за счет молекул из других источников.
метаболитом, поскольку полностью окисляется до СО2.
1.3. Обмен углеводов
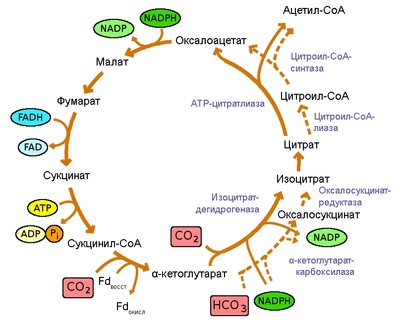
Пищевые углеводы. Схема переваривания углеводов в жкт. Причины непереносимости молока.
Пищевые углеводы — полимеры и димеры — подвергаются перевариванию в пищеварительном тракте под действием ферментов, которые гидролизуют гликозидные связи и образуют мономеры, способные всасываться, поступать в кровь, а затем в ткани
Пищевые углеводы в зависимости от химического строения разделяются на три группы:
I группа — моносахариды: глюкоза, фруктоза, галактоза.
II группа — дисахариды: сахароза, лактоза, мальтоза.
III группа — полисахариды: крахмал, инулин, гликоген.
Причиной непереносимости лактозы, или гиполактазии, является неспособность человеческого организма производить достаточно лактазы, то есть фермента, расщепляющего молочный сахар, называемый лактозой.
Источник