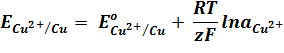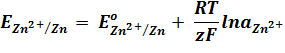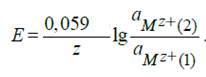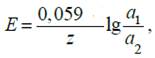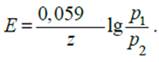Электрохимические цепи



Различают два основных вида электрохимических цепей – химические и концентрационные.
В химических цепях источником электрического тока является протекающая в системе окислительно–восстановительная химическая реакция.
Многие химические реакции являются окислительно-восстановительными. Например, при погружении цинковой пластинки в раствор сульфата меди самопроизвольно протекает реакция
в результате, которой атомы цинка окисляются, а ионы меди восстанавливаются. При таком проведении процесса энергия химической реакции превращается в тепловую энергию, но если провести процессы окисления и восстановления раздельно и осуществить передачу электронов через внешнюю цепь, можно использовать энергию химической реакции для совершения работы. В этом случае электрохимическая цепь действует как источник тока.
Гальваническими элементами ГЭ называются электрохимические цепи, в которые дают возможность получать ток за счет самопроизвольно протекающих в обычных условиях химических реакций.
Элемент (или устройство), в котором энергия химической реакции преобразуется в электрическую называется гальваническим элементом.
ГЭ состоит как минимум из 2-х электродов; на одном из которых всегда идет процесс окисления (отрицательный электрод, анод), а на другом – процесс восстановления (положительный электрод, катод).
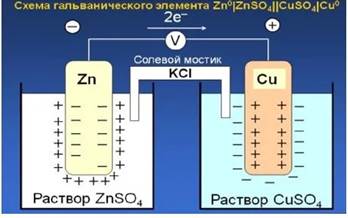
Одним из наиболее простых гальванических элементов является элемент Даниэля-Якоби, состоящий из двух электродов – цинкового и медного, погруженных в соответствующие растворы сульфатов цинка и меди, и соединенных солевым агар-агаровым мостиком.
Для устранения диффузионного потенциала растворы соединяют электролитическим мостиком, который представляет собой изогнутую стеклянную трубку наполненную насыщенным раствором электролита (например КСl), у которого подвижности К + и А — приблизительно равны. Агар-агар используют для того, чтобы удержать электролит в трубке.
Цинковый электрод по отношению к медному заряжается отрицательно. При замыкании внешней цепи цинк растворяется, происходит реакция окисления:
а на медном электроде — восстановления:
Движение потока электронов по проводнику – это и есть электрический ток.
Общий процесс является суммой процессов, протекающих на отдельных электродах:
Для ГЭ принята следующая форма записи электрохимической цепи:
· Cлева записывается электрод имеющий более отрицательный потенциал (анод),
· справа – электрод, имеющий более положительное значение потенциала (катод).
· по краям цепей записываются Ме (материал электрода). Вертикальная линия обозначает границу раздела фаз Ме – раствор. Растворы обоих электродов отделяются двумя сплошными линиями, обозначающими отсутствие диффузионного потенциала (Δφдиф = 0).
Электродные полуреакции принято записывать как реакции восстановления. Поэтому общая реакция в ГЭ записывается как разность между реакциями на правом и левом электродах: слева записываются вещества в окисленной форме и электроны, справа – вещества в восстановленной форме.
Правый электрод: Cu 2+ + 2ē → Cuº.
Левый электрод: Zn 2+. + 2ē → Znº
Общая реакция: Znº + Cu 2+ → Zn 2+ + Cuº.
Важной характеристикой ГЭ является его электродвижущая сила (ЭДС). Электродвижущая сила элемента равна разности потенциалов на концах правильно разомкнутой равновесной цепи. ЭДС обозначают E, которую рассчитывают по формуле:
где Е+ и Е– — потенциал положительного и отрицательного электродов соответственно.
Е о = Е о + – Е о –,
где Е о + и Е о – — стандартный потенциал положительного и отрицательного электродов соответственно
Электрохимическая цепь называется правильно разомкнутой, если она начинается и заканчивается одним и тем же металлом. В системе СИ ЭДС измеряется в вольтах.
ЭДС всегда положительна, поскольку она соответствует определенному самопроизвольно протекающему процессу, дающему положительную работу. ЭДС цепи отражает все процессы, происходящие на границе раздела фаз в равновесной цепи.
Для гальванического элемента Даниэля – Якоби ЭДС равна:
Согласно уравнению Нернста
Вычитая второе уравнение из первого, получим выражение для ЭДС медно-цинкового гальванического элемента:
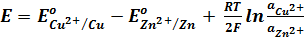
Для любого другого элемента, в основе работы которого лежит химическая реакция, ЭДС может быть вычислена по уравнению:
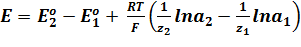
E o 1 и E o 2 – стандартные потенциалы электродов;
z1 z2 – зарядовые числа ионов;
a1 a2 – активности ионов в растворе.
Записать схему цепи, составленной из цинкового и хлорсеребряного электродов. Определить стандартную ЭДС цепи.
Выпишем из справочника электродные полуреакции (потенциалопределяющие) и стандартные потенциалы электродов:
Стандартная ЭДС рассчитывается по Е о = Е о + – Е о –.
Положительным в цепи будет тот электрод, который имеет больший условный потенциал. Положительным будет хлорсеребряный электрод, отрицательным – цинковый.
Е о = E o Сl ̅ / AgCl, Ag – E o Zn2+/Zn = 0,222 – (–0,763) = 0,985 В.
Схема цепи Zn | Zn 2+ | | Сl ̅ | AgCl, Ag
Реакции в гальваническом элементе:
| Катод | Сl ̅ | AgCl, Ag | AgCl + e = Agº + Cl – |
| Анод | Zn 2+ | Zn | Zn 2+. + 2ē → Znº |
| Суммарная реакция |