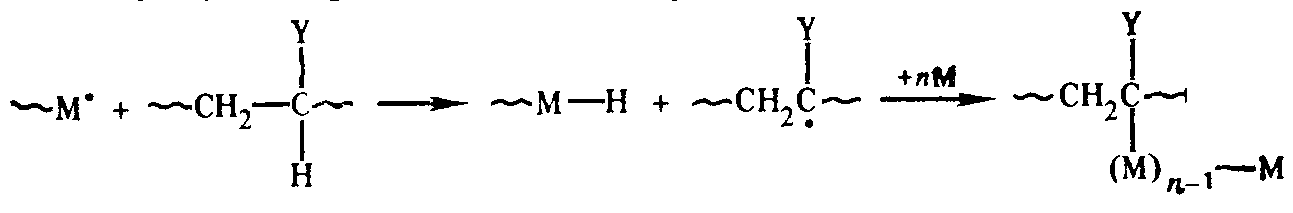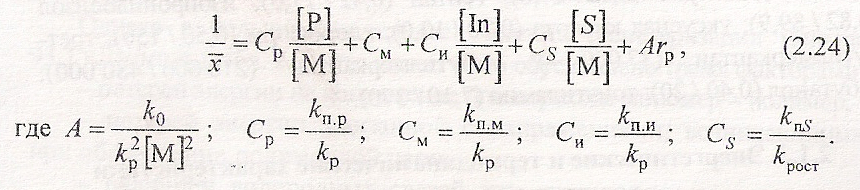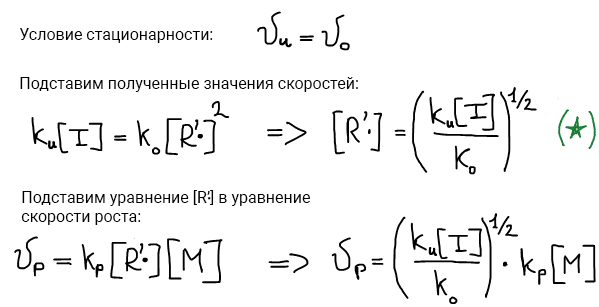- Передача цепи через растворитель, мономер, инициатор, регулятор мм полимера.
- Реакции передачи цепи при радикальной полимеризации.
- Радикальная полимеризация: механизм, кинетика и термодинамика
- Механизм реакции
- I. Инициирование цепи (зарождение)
- Физическое инициирование
- Химическое инициирование
- Примеры инициаторов:
- II. Рост Цепи
- III. Обрыв цепи
- IV. Передача цепи
- Кинетика радикальной полимеризации
- I. Влияние концентрации исходных веществ на скорость реакции.
- II. Влияние концентрации исходных веществ на степень полимеризации.
- III. Влияние температуры на скорость реакции роста цепи.
- IV. Влияние температуры на степень полимеризации.
- V. Влияние давления на скорость полимеризации
- Ингибиторы и замедлители полимеризации.
- Термодинамика радикальной полимеризации
- Влияние температуры
- Термодинамическая вероятность
Передача цепи через растворитель, мономер, инициатор, регулятор мм полимера.
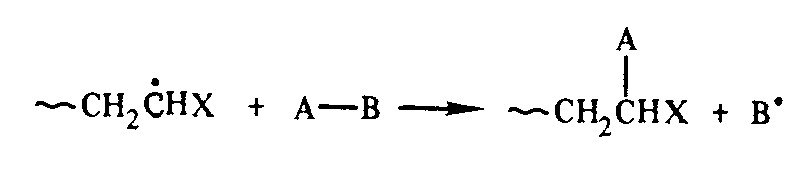
Передача цепи – процесс, осложняющий радикальную полимеризацию. Передача цепи происходит к результате реакции растущих макрорадикалов с соединениями, содержащими связи, способные к взаимодействию с радикалами. Молекула соединения А-В отдает макрорадикалу тог иди иной атом и превращается в новый радикал, инициирующий возникновение новой полимерной цепи:
Если радикал В* активен, то общая скорость полимеризации не изменяется, кинетическая цепь сохраняется, а материальная распадается на несколько более коротких пеней с образованием макромолекул более низкой молекулярной массы. Передача цели может происходить следующими способами:
1. Передача цепи через растворитель — происходит чаще всего путем отрыва макрорадикалом от молекулы растворителя атомов водорода или галогена:
Образовавшиеся радикалы инициируют дальнейшую полимеризацию мономера. Скорость реакции равна: rп.р=kп.р [R*][P]
где kп.р — константа скорости реакции передачи цепи через растворитель; [P] — концентрация раствори геля, моль/л.
Средняя степень полимеризации макромолекул, образующихся в результате передачи цепи через растворитель, равна: xп.р ср = rp/rп.р
2. Передача цепи через мономер — возможна, если молекулы последнего содержат подвижные атомы (Н, CI, Вг, и т. д.), способные к взаимодействию с растущими макромолекулами:
Образовавшийся радикал инициирует полимеризацию оставшегося мономера:
Скорость передачи цепи через мономер определяется по уравнению:
Средняя степень полимеризации равна:
3. Передача цепи через инициатор — происходит тогда, когда молекулы инициатора содержат способные к взаимодействию с растущими радикалами активные связи (чаще те, которые при распаде и образуют инициирующие радикалы). Например, при использовании гидроперекиси третбутила передача цепи через инициатор идет по схеме
В то же время передача цепи через динитрил азодиизомасляной кислоты не осуществляется.
4. Передача цепи на полимер — имеет место при высоких конверсиях и образует разветвленный продукт:
Доля реакций передачи цепи на полимер небольшая.
Константа передачи цени на полимер (Сп) для полистирола и полиметилметакрилата составляет около 10 -14 . Согласно Флори:
где ρ- плотность ветвления; р — степень завершенности реакции.
Например, в полистироле (при р = 80%) одно ветвление приходится на каждые 4-10 тыс. мономерных звеньев при средней молекулярной массе 10 5 -10 6 , т. е. одно ветвление приходится на 10 макромолекул полистирола. Реакционноспособные макрорадикалы дают более высокую степень ветвления, обусловленную реакциями передачи цепи на полимер. Высокое значение С„ для поливинилацетата обусловлено участием в передаче цепи ацетатной группы. Полиэтилен высокого давления содержит до 30 ветвей на 500 мономерных звеньев длиной С2
5. Передача цепи через специальные добавки (регуляторы, замедлители) — используется для регулирования молекулярной массы полимеров.
Скорость передачи цепи на регулятор S равна:
где kпs — константа скорости передачи цепи на регулятор.
Суммарную величину обратной степени полимеризации получают по уравнению:
Уравнение позволяет экспериментально определить константы передачи цепи на растворитель (Ср), мономер (См), инициатор (Си) и регулятор (СS). Например, См определяют при полимеризации в массе (Ср = 0) без регулятора (СS = 0) и с инициатором, не способным к передами цепи (Cи = 0). Тогда:
Источник
Реакции передачи цепи при радикальной полимеризации.
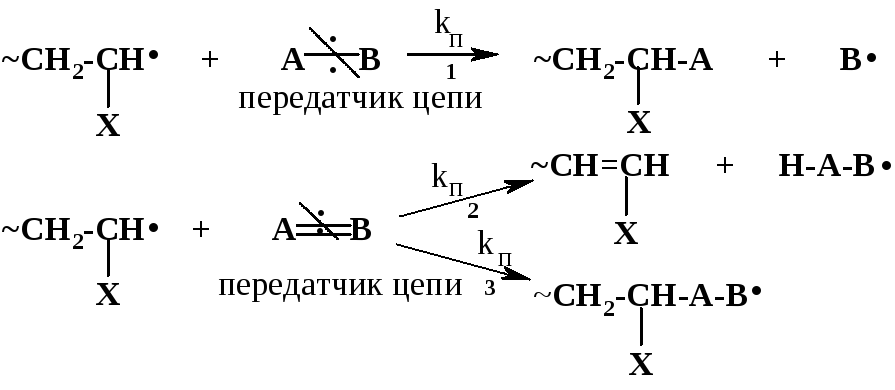
Пожалуй, наиболее часто реакции идут по схеме 1. В зависимости от мономера и присутствия передатчиков реакции передачи цепи могут играть разную роль – от относительно небольшой до доминирующей.
Следствием передачи цепи по схемам 1 и 2 является обрыв молекулярной цепи при сохранении кинетической (т.е. активного центра). Таким образом, эти реакции ведут к уменьшению длины полимерной цепи, т.е. молекулярной массы полимера. Это уменьшение тем больше, чем чаще идут реакции передачи цепи; степень этого уменьшения может меняться в весьма широких пределах – вплоть до полного ингибирования полимеризации. Степень участия реакций передачи цепи на тот ли иной агент выражается константой передачи цепи, равной отношению констант скоростей передачи цепи (kп) и роста цепи (kр):
Как влияют процессы передачи цепи на скорость полимеризации? Это зависит от характера того радикала, который образуется при передаче цепи. Здесь возможны два основных варианта:
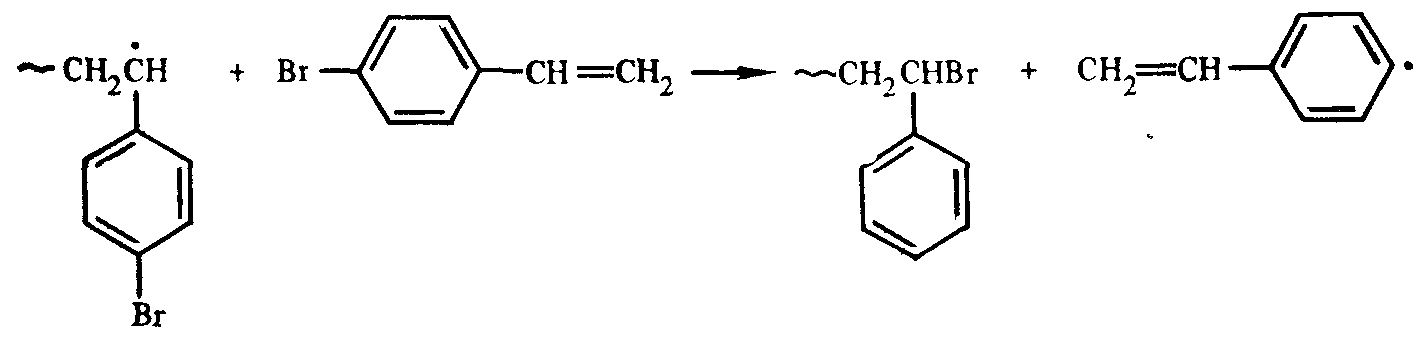
1) При передаче цепи возникает активный радикал, который способен легко присоединяться к мономеру. В этом случае он и присоединяется к мономеру и тем самым инициирует новую молекулярную цепь, например, для передачи по пути 1:

2) Радикал, возникший при передаче цепи, малоактивен или совсем неактивен; он либо с трудом присоединяется к мономеру, либо вовсе не присоединяется к нему. В этом случае скорость полимеризации уменьшается. Если такие реакции передачи идут очень легко (Сп>>1), а возникший радикал не способен присоединяться к мономеру, то агент передачи «перехватывает» радикалы, возникшие из инициатора (или образовавшиеся иным путем), и полимеризация вообще не происходит – она ингибируется. Возникшие малоактивные радикалы либо существуют как таковые (если они долгоживущие), либо подвергаются рекомбинации или диспропорционированию; таким образом, вслед за передачей цепи следует непосредственно обрыв кинетической цепи.
В качестве передатчиков цепи могут выступать: 1) молекулы инициатора; 2) молекулы мономера; 3) молекулы посторонних веществ (случайно попавших или специально введенных в реакционную смесь); 4) макромолекулы «мертвого» полимера.
1) Передача цепи на инициатор. Эта реакция может происходить при использовании пероксидных инициаторов:
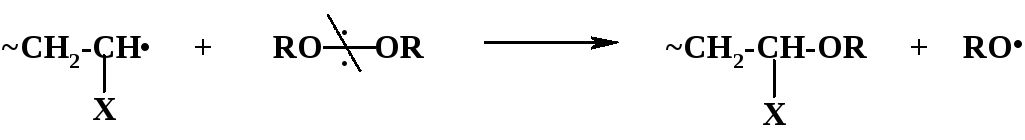
2) Передача цепи на мономер. Это – реакции взаимодействия «живой» цепи с мономером, идущие не по схеме роста цепи. Наиболее типичный вариант – передача атома водорода от растущей («живой») цепи к молекуле мономера:
Э
Источник
Радикальная полимеризация: механизм, кинетика и термодинамика
Радикальная полимеризация — процесс получения ВМС из низкомолекулярных соединений без выделения побочных продуктов, где активный центр — свободно-радикальная частица (частица с неспаренным электроном). Данный процесс осуществляется за счет кратных связей ( С = С С=С С = С , С = О С=О С = О и др.) или раскрытия циклов, содержащих гетероатомы ( N N N , S S S , O O O ).
Продукты полимеризации имеют тот же элементный состав, что и исходные мономеры.
Механизм реакции
В реакцию полимеризации вступают соединения, которые содержат по крайней мере одну кратную связь или циклы. Реакционная способность мономера зависит от его строения, сопряжения двойной связи в молекуле мономера, количества и взаимного расположения заместителей, их поляризационного явления на двойную связь.
Радикальная полимеризация протекает по цепному механизму и описывается кинетикой неразветвленной цепной реакции.
Основные стадии цепной реакции:
- Инициирование — образование активных центров;
- Рост цепи — последовательное присоединение мономеров к активному центру;
- Обрыв цепи — гибель активного центра;
- Передача цепи — передача активного центра на другую молекулу.
I. Инициирование цепи (зарождение)
Данная стадия является самой энергоемкой. Различают физическое и химическое инициирование.
Физическое инициирование
Термоинициирование — инициирование при высоких температурах.
Фотоинициирование — инициирование под действием света.
Использование лучей высокой энергии —
Механоинициирование — инициирование в результате удара.
Химическое инициирование
Данный способ инициирования применяется чаще всего. Принцип заключается в использовании веществ-инициаторов (перекиси, азосоединения, red-ox системы), у которых энергия обрыва химической связи значительно меньше, чем у мономеров. При этом процесс происходит в две стадии: сначала генерируются радикалы инициатора, которые затем присоединяются к молекуле мономера, образуя первичный мономерный радикал.
Инициатор очень похож по свойствам на катализатор, но его отличие состоит в том, что инициатор расходуется в процессе химической реакции, а катализатор — нет.
Примеры инициаторов:
Динитрил азобисизомасляной кислоты
Соли металлов переменной валентности (ОВР)
II. Рост Цепи
Мономеры поочередно присоединяются к активному центру первичного мономерного радикала.
III. Обрыв цепи
Обрыв цепи происходит в результате гибели активных центров (обрыв кинетической цепи).
- Обрыв кинетической цепи — исчезают активные центры;
- Обрыв материальной цепи — когда данная цепь перестает расти, но активный центр передается другой макромолекуле или мономеру (реакция передачи цепи).
Реакции приводящие к гибели кинетической и материальной цепи – реакции рекомбинации и диспропорционирования.
Вид реакции обрыва цепи (рекомбинация или диспропорционирование) зависит от ряда факторов, в частности от строения молекулы мономера. Если мономер содержит громоздкий по размеру или электроотрицательный по химической природе заместитель, то столкновения таких растущих радикалов друг с другом не происходит и обрыв цепи осуществляется путем диспропорционирования. Например, в случае метилметакрилата:
По мере роста радикалов увеличивается вязкость системы, и вследствие подвижности макрорадикалов скорость обрыва цепи путем рекомбинации снижается. Рост времени жизни макрорадикалов при увеличении вязкости системы приводит к интересному явлению – ускорению полимеризации на поздних стадиях (гель-эффект) вследствие увеличения концентрации макрорадикалов.
IV. Передача цепи
Передача цепи происходит путём отрыва растущим радикалом атома или группы атомов от какой-то молекулы . Реакция передача цепи приводит к обрыву материальной цепи, а рост кинетической продолжается.
через полимер — приводит к получению разветвленных полимеров (ухудшение свойств полимеров)
через растворитель — приводит к получению полимеров с меньшей молекулярной массой
через мономер — обрывается материальная цепь, продолжается кинетическая
Особенности радикальной полимеризации:
- Высокая скорость полимеризации;
- Разветвленность;
- Возможны присоединения г-г, г-хв, хв-хв;
- Полимолекулярные полимеры.
Кинетика радикальной полимеризации
Химическая кинетика — это раздел химии, изучающий механизм и закономерности протекания химической реакции во времени, зависимости этих закономерностей от внешних условий.
Для изучения кинетики радикальной полимеризации необходимо рассмотреть зависимость скорости реакции и степени полимеризации от концентрации исходных веществ, давления и температуры.
I. Влияние концентрации исходных веществ на скорость реакции.
Общая скорость реакции зависит от скорости образования радикалов Vин (скорости инициирования) , от скорости роста цепи Vр и ее обрыва Vo.
Мы будем рассматривать реакцию свободнорадикальной полимеризации, когда инициирование осуществляется с помощью химических инициаторов.
Рассмотрим каждую стадию:
Рассмотрение кинетики существенно облегчается, если реакция протекает в условиях, близких к стационарному режиму, при котором скорости возникновения и исчезновения свободных радикалов можно считать равными. При этом концентрация активных центров будет постоянна.
Как видно из графика кривой можно выделить пять участков по значениям скоростей основной реакции превращения мономера в полимер в результате полимеризации:
1 — участок ингибирования, где концентрация свободных радикалов мала. И они не могут начать цепной процесс полимеризации;
2 — участок ускорения полимеризации, где начинается основная реакция превращения мономера в полимер, причем скорость растет;
3 — участок стационарного состояния, где происходит полимеризация основного количества мономера при постоянной скорости (прямолинейная зависимость конверсии от времени);
4 — участок замедления реакции, где скорость реакции уменьшается в связи с убылью содержания свободного мономера;
5 — прекращение основной реакции после исчерпания всего количества мономера.Стационарный режим наблюдается обычно на начальной стадии протекания реакции, когда вязкость реакционной массы невелика и равновероятны случаи зарождения цепи и ее обрыва.
Таким образом скорость реакции роста цепи равна:
II. Влияние концентрации исходных веществ на степень полимеризации.
Степень полимеризации зависит от соотношения скоростей роста и обрыва цепи:
Учтем соответствующие выражения для скоростей
Степень полимеризации равна:
III. Влияние температуры на скорость реакции роста цепи.
Выполним подстановку уравнения Аррениуса в уравнение скорости роста цепи:
Прологарифмируем полученное выражение:
Энергия активации инициирования
Числитель (6+15-4 = 17) больше нуля, значит, чем больше температура, тем выше скорость реакции радикальной полимеризации. Однако с ростом температуры увеличивается и вероятность столкновения радикалов друг с другом (обрыв цепи путем диспропорционирования или рекомбинации) или с низкомолекулярными примесями. В результате молекулярная масса полимера в целом уменьшается, увеличивается доля низкомолекулярных фракций в полимере. Возрастает число побочных реакций, приводящих к образованию разветвленных молекул. Увеличивается нерегулярность при построении цепи полимера вследствие возрастания доли типов соединения мономера «голова к голове» и «хвост к хвосту».
IV. Влияние температуры на степень полимеризации.
Энергия активации инициирования
Числитель (6-15-4 = -13) меньше нуля, значит с ростом температуры степень полимеризации уменьшается. В результате молекулярная масса полимера в целом уменьшается, увеличивается доля низкомолекулярных фракций в полимере.
V. Влияние давления на скорость полимеризации
Принцип Ле-Шателье: Если на систему оказывается внешнее воздействие, то в системе активируются процессы, ослабляющие это воздействие.
Чем выше давление, тем выше скорость радикальной полимеризации. Однако чтобы повлиять на свойства конденсированных систем, нужно прикладывать давление в несколько тысяч атмосфер.
Особенностью полимеризации под давлением является то, что увеличение скорости не сопровождается уменьшением молекулярной массы получаемого полимера.
Ингибиторы и замедлители полимеризации.
Явления обрыва и передачи цепи широко используются на практике для:
- предотвращения преждевременной полимеризации при хранении мономеров;
- для регулирования процесса полимеризации
В первом случае к мономерам добавляют ингибиторы или стабилизаторы, которые вызывают обрыв цепи, а сами превращаются в соединения, не способные инициировать полимеризацию. Также они разрушают пероксиды, образующиеся при взаимодействии мономера с атмосферным кислородом.
Ингибиторы: хиноны, ароматические амины, нитросоединения, фенолы.
Регуляторы полимеризации вызывают преждевременный обрыв материальной цепи, снижая молекулярную массу полимера пропорционально введенному количеству регулятора. Примером их являются меркаптаны.
Термодинамика радикальной полимеризации
Реакция роста цепи обратима, наряду с присоединением мономера к активному центру может происходить и его отщепление-деполимеризация.
Термодинамическая возможность полимеризации, как и любой другой равновесный химический процесс можно описать с помощью функций Гиббса и Гельмгольца:
Однако функция Гиббса наиболее приближена к реальным условиям, поэтому мы воспользуемся ей:
Так же изменение функции Гиббса связано с константой равновесия реакции уравнением:
Константа полимеризационно-деполимеризационного равновесия при достаточно большом молекулярном весе образующегося полимера (p>>1) зависит только от равновесной концентрации мономера:
Из уравнения (а) можно найти такую температуру, при которой реакция полимеризации не будет идти, а из уравнения (б) можно найти равновесную концентрацию мономера, при превышении которой будет происходить полимеризация.
Влияние температуры
Для определения влияния температуры на равновесную концентрацию мы представим уравнение (б) в следующем виде:
В случае, когда ΔH° 0 и ΔS°>0 наблюдается обратная зависимость: с уменьшением температуры увеличивается равновесная концентрация мономера. Следовательно, для мономеров с отрицательным тепловым эффектом существует нижняя предельная температура Тн.пр.
Так же есть известные случаи, когда эти зависимости не пересекаются, но они не представляют практического интереса.
Термодинамическая вероятность
Теперь рассмотрим термодинамическую возможность протекания реакции, условием которой является равенство ΔG 0)
Рост цепи (ΔS2°
Источник